
Salud
Cómo será el ensayo del suero hiperinmune en el Güemes y quiénes pueden participar
27/07/2020 |
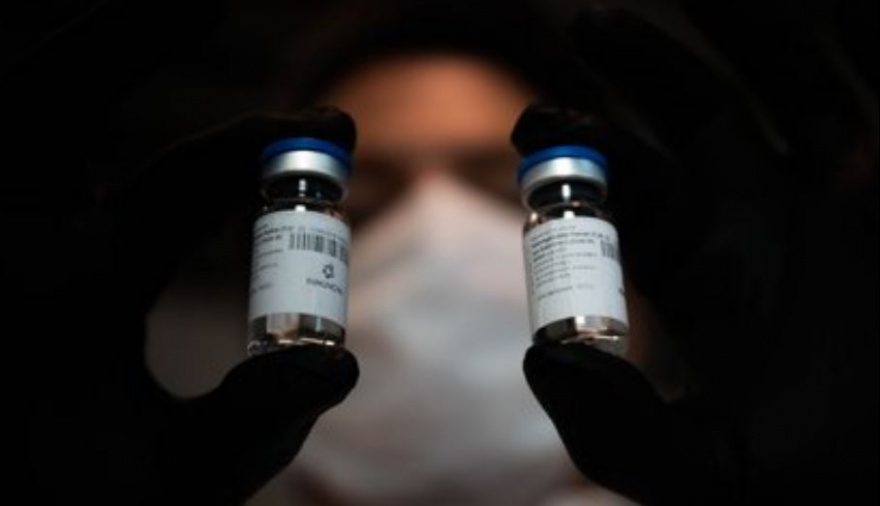
Tras la aprobación de la ANMAT para iniciar las pruebas en seres humanos, el Sanatorio Güemes es el primer centro que calificó para iniciarlas.El coordinador del estudio explicó los detalles a Infobae
Por Agustina D´Ambra
El viernes 24 de julio se conoció la aprobación de la ANMAT para lel estudio clínico del suero equino hiperinmune, un tratamiento de los más avanzados contra la enfermedad COVID-19 que causó la pandemia actual.
De este modo, el suero equino hiperinmune se sumó oficialmente a otros tratamientos en estudio en humanos que están en experimentación, como el uso de antiinflamatorios, los antivirales, plasma de convalecientes y más.PUBLICIDAD
El estudio clínico comenzará a realizarse está semana en el Sanatorio Güemes, en el Hospital General de Agudos “Dr. Ignacio Pirovano”, ambos de CABA, en el Hospital Cuenca Alta - SAMIC de Cañuelas y en el Instituto Médico Platense de La Plata. Próximamente iniciará en más de diez hospitales y clínicas de obras sociales del área metropolitana de Buenos Aires y La Plata.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/7FX3GNTYE5GUZD2WDMJDBCMQRA.jpg) El estudio incluye la participación voluntaria de 242 pacientes adultos con enfermedad moderada a severa causada por la infección del SARS-CoV-2 confirmada por PCR
El estudio incluye la participación voluntaria de 242 pacientes adultos con enfermedad moderada a severa causada por la infección del SARS-CoV-2 confirmada por PCR
Dentro de las instituciones seleccionadas, se encuentra el Sanatorio Güemes, el primer centro que calificó para iniciar las pruebas en seres humanos. De acuerdo a Anselmo Berttetti, médico especialista en medicina Interna y en Oncología Clínica y coordinador de clínica del Sanatorio Güemes, quien está a cargo del protocolo, podrán participar del ensayo aquellos pacientes que estén diagnosticados con la enfermedad del COVID-19, que presenten un cuadro de moderado a grave pero que no se encuentren en terapia intensiva.
El estudio incluye la participación voluntaria de 242 pacientes adultos con enfermedad moderada a severa causada por la infección del SARS-CoV-2 confirmada por PCR, dentro de los diez días del inicio de síntomas y que requieren hospitalización. “Al momento de reclutar a los pacientes diagnosticados se debe seleccionar aquellos que sean mayor de edad y el profesional debe explicarle en qué consiste la investigación, cuáles son los potenciales beneficios del tratamiento, el alcance del mismo y los pasos a seguir”, explicó a Infobae Bertteti.
En este sentido, el profesional a cargo, explicó que la prueba durará aproximadamente dos meses para poder tener los datos consistentes y que el martes 24 de julio tendrán la visita de inicio y estarían en condiciones de iniciar el reclutamiento para poder llevar a cabo la experimentación: “La finalidad es tratar de reducir el riesgo de que los pacientes evolucionen a patologías severas así como reducir la previsión de enfermedad y los días de internación de una persona con COVID-19″.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/SLHLTTUUKRE2XB26PGNY5KI7AE.jpg) Laboratorio Universidad San Martin - Inmunova - Suero Anticuerpos COVID 19 - Coronavirus (Foto: Franco Fafasuli)
Laboratorio Universidad San Martin - Inmunova - Suero Anticuerpos COVID 19 - Coronavirus (Foto: Franco Fafasuli)
“Estamos entusiasmados institucionalmente con la participación en este estudio ya que somos un eslabón más de la cadena que busca una respuesta a la enfermedad, y tenemos mucha ilusión porque podríamos llegar a brindar una respuesta a la problemática”, enfatizó el profesional.
Además, el especialista dijo que al ser un potencial tratamiento íntegramente desarrollado en Argentina, hay mucha expectativa para ver cómo se desenvuelve en esta nueva fase.
Dicho estudio clínico de Fase 2/3 aprobado por ANMAT busca demostrar la seguridad y eficacia del suero hiperinmune en términos de mejoría clínica del paciente: la recuperación pronta para poder ser externado, que no avance la enfermedad y, por lo tanto, la necesidad de asistencia respiratoria mecánica o el traslado a una unidad de cuidado intensivo.
Este suero terapéutico es una inmunoterapia basada en anticuerpos policlonales equinos, obtenidos mediante la inyección de una proteína recombinante del SARS-CoV-2 en estos animales, inocua para ellos, que hace que generen gran cantidad de anticuerpos neutralizantes. Luego de la extracción del plasma –un proceso similar al que se utiliza cuando se extrae plasma de personas (plasmaféresis)– estos anticuerpos se purifican y procesan, a través de un proceso biotecnológico, para obtener fragmentos de los anticuerpos con alta pureza y buen perfil de seguridad.:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/QTM6J7PZGFG2PNOUXMCGDLXJZM.jpg) Los anticuerpos policlonales equinos se utilizan para la elaboración de medicamentos, atender emergencias médicas, entre otras (Foto: Franco Fafasuli)
Los anticuerpos policlonales equinos se utilizan para la elaboración de medicamentos, atender emergencias médicas, entre otras (Foto: Franco Fafasuli)
El suero producido contiene gran cantidad de estos anticuerpos con capacidad neutralizante, es decir, que podría evitar que el virus ingrese a las células que es donde se multiplica. Ha sido desarrollado para inmunización pasiva, es decir, que al paciente se le administran anticuerpos contra el agente infeccioso, produciendo su bloqueo y evitando que se propague. Esta estrategia terapéutica es similar a la del plasma de personas que se recuperaron del COVID-19, pero en este caso los anticuerpos se obtienen de plasma equino. Esto posibilita que la producción del suero terapéutico a partir de este plasma pueda escalarse en cantidad.
Los anticuerpos policlonales equinos se utilizan para la elaboración de medicamentos, atender emergencias médicas como el envenenamiento por mordedura de serpientes y alacranes, intoxicaciones por toxina tetánica, botulismo, exposición al virus de la rabia y enfermedades infecciosas como la influenza aviar.
Este posible tratamiento para hacer frente al COVID-19 es fruto del trabajo encabezado por Inmunova y el Instituto Biológico Argentino (BIOL), con la colaboración de la Administración Nacional de Laboratorios e Institutos de Salud “Dr. Carlos G. Malbrán” (ANLIS), Fundación Instituto Leloir (FIL), Mabxience, CONICET, Universidad Nacional de San Martín (UNSAM), Instituto de Virología “Dr. José M. Vanella” de la Universidad Nacional de Córdoba y Grupo Insud. Y cuenta con el apoyo de la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación.















